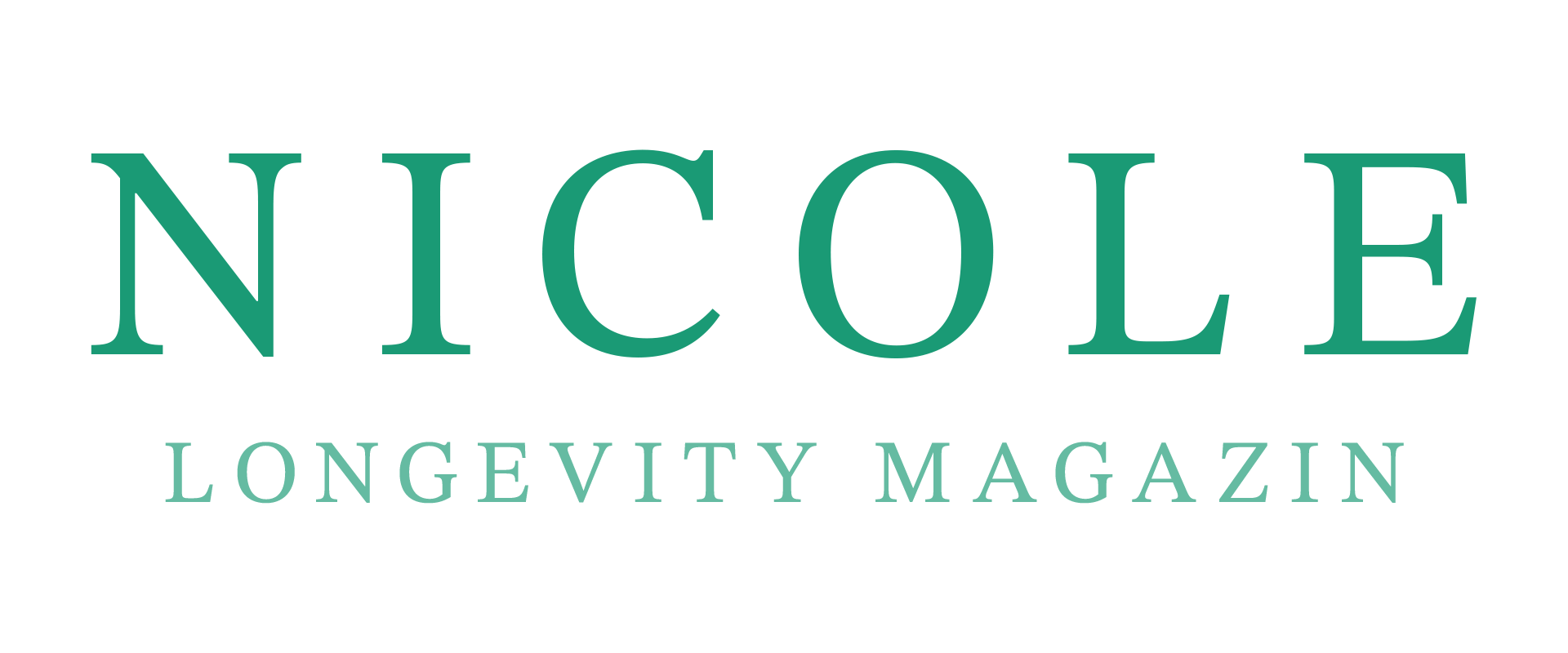A gyógyszerek világa mindig is az apró részleteken múlt. Egyetlen atom helyzete dönthetett életről vagy halálról, gyógyulásról vagy kudarcba fulladt reményekről. A hagyományos gyógyszerfejlesztés során a tudósok úgy alkottak, mint ékszerészek: minden kötés, minden szög tökéletesen megkomponált volt. Most azonban valami még nagyobb dolog kapott szárnyra: a nanomedicina.
A gyógyszer hatékonysága és biztonságossága szorosan összefüggött a szerkezeti precizitással. Egyetlen atom helyzete dönthet arról, hogy egy molekula hatásos gyógyszer lesz-e, vagy hatástalan marad. Ez az elv formálta a kis molekulájú gyógyszerek történetét – ám most a Northwestern Egyetem és a Mass General Brigham kutatói szerint1 a jövő terápiái akkor lehetnek igazán hatékonyak és biztonságosak, ha ugyanilyen molekuláris precizitással készülnek, amely eddig csak a kis molekulájú gyógyszerek világában volt elképzelhető.
A jelenlegi nanogyógyszerek – köztük az mRNS-alapú vakcinák – még jelentős strukturális eltéréseket mutatnak egy-egy adagban, ami befolyásolhatja a hatásosságot és a biztonsági profilt. A cél az, hogy minden részecske szerkezete pontosan kontrollált legyen.
Struktúra, ami meghatározza a hatást
A nanogyógyszerek hatása nemcsak a kémiai összetételtől, hanem az összetevők nanoszintű elrendezésétől is függ. A gondosan szervezett struktúrák képesek fokozni a terápiás hatékonyságot, célzottabb beavatkozást biztosítani, és egyben csökkenteni a nem kívánt mellékhatásokat. Lehetővé teszi, hogy a nanogyógyszerek még célzottabban, még biztonságosabban lépjenek kapcsolatba az emberi szervezettel.
Ez a megközelítés utat nyithat olyan betegségek gyógyításához, mint a rák, a fertőző betegségek, a neurodegeneratív kórképek és az autoimmun zavarok.
„A nanogyógyászat strukturális alapokra helyezése paradigmaváltást jelent. Ha a terápiás összetevők elrendezését is ugyanazzal a gondossággal tervezzük meg, mint korábban az atomokat a kis molekulákban, akkor hatékonyabb, célzottabb és biztonságosabb gyógymódokat alkothatunk” – hangsúlyozza Chad A. Mirkin professzor, a Northwestern Egyetem világszerte elismert nanogyógyászati úttörője.
Megérkezett a strukturált nanogyógyászat
A hagyományos vakcinák és immunterápiák jellemzően egy „keverék” elven működtek: antigéneket és adjuvánsokat kevertek össze anélkül, hogy azok szerkezetét szisztematikusan szabályozták volna. Ezzel szemben a strukturált nanogyógyszerek a komponenseket pontos térbeli rendbe szervezik, így fokozzák a terápiás hatékonyságot és csökkentik a mellékhatásokat.
A kihívás abban rejlik, hogy jelenleg a nanogyógyszerek változékonysága magas: az egyes részecskék mérete, összetétele és felületi jellemzői eltérhetnek. Ez bizonytalansághoz vezethet a terápiás hatásban is. A kutatók ezért egy új korszak felé nyitnak: az atomok szintjén is szabályozott szerkezetek felé.
„Mirkin professzor szerint A szerkezet szabályozásával olyan új terápiás platformokat hozhatunk létre, amelyek messze túlszárnyalják a hagyományos DNS- és RNS-alapú megközelítéseket”
A kutatók három úttörő példát emelnek ki a strukturális nanogyógyászatból:
- Gömbös nukleinsavak (SNA-k): Olyan speciális DNS-szerkezetek, amelyek könnyen bejutnak a sejtekbe, és bizonyítottan hatékonyabbak a lineáris DNS-eknél például génterápiában és vakcinafejlesztésben. Klinikai vizsgálatokban még halálos bőrrák gyógyításában is áttörést értek el.
- Kemoflare-ok: Olyan intelligens nanoszerkezetek, amelyek a daganatsejtek jelzéseire válaszolva szabadítják fel a kemoterápiás hatóanyagokat.
- Megamolekulák: Professzionálisan felépített fehérjeszerkezetek, amelyek az antitestek működését imitálják, és többféle terápiás vagy diagnosztikai funkciót képesek egyszerre ellátni.
Intelligens terápiák
„A következő generációs nanogyógyszerek képesek lesznek a betegségek szövet- és sejtszintű jeleit felismerve célzottan és időzítve felszabadítani a hatóanyagokat. Ez drámai módon növelheti a terápiás hatékonyságot, miközben minimalizálja a szisztémás mellékhatásokat” – mutat rá Natalie Artzi professzor, a strukturális nanogyógyászat egyik vezető alakja.
A strukturális nanogyógyászat nemcsak a jelen, hanem a jövő orvostudományának is az alapját képezheti
Ám a kutatások egyre szélesebb horizontot tárnak fel: a nanotechnológia nemcsak a gyógyszermolekulák szintjén, hanem az egész emberi szervezetben forradalmasíthatja az orvoslást.
A jövő egyik legizgalmasabb víziója az emberi test és a nanotechnológia szoros integrációja, ahol bio-nano interfészek és nanobotok segíthetik a belső folyamatok monitorozását és finomhangolt szabályozását. Ezek az intelligens rendszerek képesek lehetnek a betegségek korai felismerésére, a célzott gyógyszerfelszabadításra, a szövetek regenerációjának támogatására, sőt, az öregedési folyamatok lassítására is!
A molekuláris szintű kommunikáció – ahol a sejtek és a nanotechnológiai eszközök közvetlen párbeszédet folytatnak – új dimenziókat nyithat a személyre szabott orvoslásban. A bio-nano interfészek fejlesztése lehetővé teheti, hogy a terápiás beavatkozások valós időben igazodjanak a szervezet állapotához, még a sejtszintű változások megjelenése előtt.
A mesterséges intelligencia szerepe a jövő tervezésében
A molekuláris szintű tervezés óriási lehetőségeket, de egyben hatalmas komplexitást is rejt: tízezernyi lehetséges szerkezeti variáció közül kell kiválasztani a legjobbat, s ennél a lépésnél lép be a képbe a mesterséges intelligencia, mivel az AI-alapú algoritmusok segítenek leszűkíteni a lehetőségeket, felgyorsítva a szintézist és a kísérleti tesztelést.
A szerkezeti precizitás nem pusztán technológiai kérdés: alapjaiban formálja át azt, hogyan tervezünk gyógyszereket a jövőben. A nanogyógyászat következő nagy lépése a molekuláris szintű rend létrehozása – és ezzel a hosszú, egészséges élet új lehetőségeinek megteremtése.